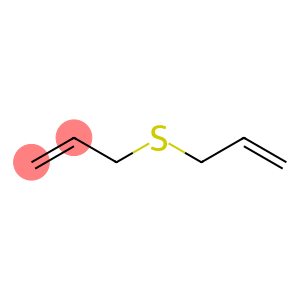
sulfur d'al·lil (CAS #592-88-1)
| Símbols de perill | Xi – Irritant |
| Codis de risc | R10 - Inflamable R36/37/38 – Irrita els ulls, el sistema respiratori i la pell. |
| Descripció de seguretat | S26 – En cas de contacte amb els ulls, esbandiu immediatament amb aigua abundant i consulteu un metge. S36 - Utilitzar roba de protecció adequada. S37/39 - Utilitzeu guants adequats i protecció ocular/cara S23 – No respirar els vapors. S16 - Mantenir allunyat de fonts d'ignició. |
| ID de l'ONU | ONU 1993 3/PG 3 |
| WGK Alemanya | 2 |
| RTECS | BC4900000 |
| TSCA | Sí |
| Codi HS | 29309070 |
| Classe de perill | 3 |
| Grup d'embalatge | III |
Introducció
El sulfur d'alil és un compost orgànic. Té les següents propietats:
Propietats físiques: El sulfur d'allil és un líquid incolor amb una forta olor picant.
Propietats químiques: El sulfur d'al·lil és capaç de reaccionar amb molts compostos, especialment reactius amb electrofilicitat, com ara halògens, àcids, etc. Pot patir reaccions de polimerització en determinades condicions.
Principals usos del sulfur d'alil:
Com a intermedi: el sulfur d'alil es pot utilitzar com a intermedi en la síntesi orgànica i participar en una sèrie de reaccions de síntesi orgànica, per exemple, es pot utilitzar per sintetitzar haloolefines i compostos heterocíclics d'oxigen.
Hi ha diversos mètodes principals per a la preparació de sulfur d'alil:
Reacció de substitució d'hidrotiol: el sulfur d'alil es pot formar per reaccions com el bromur d'alil i l'hidrosulfur de sodi.
Reacció de conversió de l'alcohol al·lílic: es prepara per la reacció de l'alcohol al·lílic i l'àcid sulfúric.
Des d'una perspectiva de seguretat, el sulfur d'al·lil és una substància irritant que pot causar irritació i danys en contacte amb la pell i els ulls. Eviteu el contacte directe amb la pell i els ulls quan utilitzeu i mantingueu bones condicions de ventilació. El sulfur d'alil és volàtil i s'ha d'evitar en cas d'exposició prolongada a altes concentracions de vapors o gasos.